Stanowisko konsultanta: Stosowanie preparatu Evusheld
Szanowni Państwo,
W związku z informacjami z FDA, uprzejmie informuję, że stosowanie preparatu Evusheld naszych pacjentów jest uzasadnione.
Z wyrazami szacunku
Jan Styczyński
Informacja FDA:
Preparat Evusheld nie jest obecnie dopuszczony do stosowania w ramach procedury Emergency Use Authorization (FDA) jako forma profilaktyki przedekspozycyjnej COVID-19 w Stanach Zjednoczonych u osób z zaburzeniami odporności. Powodem takiej decyzji jest wzrost powyżej 90% udziału wariantów wirusa SARS-CoV-2, które nie są neutralizowane przez Evusheld. FDA poinformowała, że w sytuacji, kiedy udział wariantów wirusa, których Evusheld nie neutralizuje spadnie poniżej 90%, podejmie decyzję w zakresie przywrócenia pozwolenia stosowania preparatu w profilaktyce przedekspozycyjnej COVID-19 u osób z zaburzeniami odporności: www.fda.gov
Dane dla poszczególnych krajów mogą znacząco różnić się od siebie. Według danych dostępnych w dniu 30.01.2023 (raport GISAID z dn. 16.01.2023) udział w Polsce wariantów neutralizowanych przez Evusheld wynosi 42% (34% BA.5 i 8,2% BA.2.75), a w Niemczech 52%: www.ourworldindata.org . Sytuacja dynamicznie się zmienia, dane z różnych krajów spływają w różnym czasie, obecnie dostępne dane z raport GISAID z dn. 03.02.2023 pokazują iż w Niemczech właściwości neutralizujące utrzymują się w odniesieniu do 47% (26% BA.5 i 21% BA. 2.75), polskie dane nie zostały jeszcze zaktualizowane.
Ze względu na dużą zmienność i różnorodność występowania wariantów wirusa SARS-CoV-2 w poszczególnych krajach – zgodnie z wytycznymi europejskich organów ds. zdrowia publicznego – prowadzone jest bieżące monitorowanie sytuacji epidemiologicznej i wpływ przy podejmowaniu decyzji terapeutycznych.
Neutralizacja podwariantów Omicron dla produktu Evusheld przedstawia się następująco:
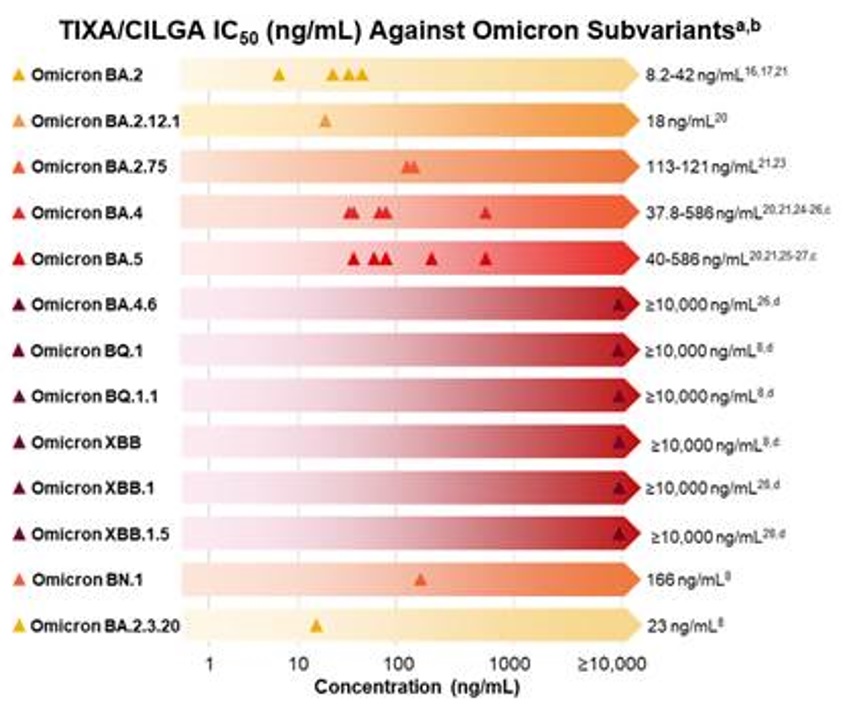
aLive and pseudovirus neutralization assays;
bSome data points presented are EC50 values, which represent the concentration of a drug that produces 50% of the maximum possible effect
